Tumori: per il 2025 si stima una diminuzione dei tassi di mortalità.
Per il cancro alla mammella è previsto un calo generale, ma un aumento tra le pazienti più anziane
Le previsioni dei decessi per tumori indicano una diminuzione dei tassi di mortalità del 3,5% circa nell’Unione Europea negli uomini e dell’1,2% nelle donne. Un andamento positivo è stimato anche per il tumore della mammella, tranne nelle donne ultraottantenni, probabilmente per mancanza di screening regolari, diagnosi tempestive e utilizzo di terapie innovative. I risultati dello studio, coordinato dall’Università degli Studi di Milano in collaborazione con l’Università di Bologna e sostenuto dalla Fondazione AIRC, sono stati pubblicati sulla rivista “Annals of Oncology”.
Milano, 12 marzo 2025 – Nel 2025 i tassi di mortalità per tumore della mammella dovrebbero diminuire in tutte le fasce d’età nell’Unione Europea (UE), a eccezione delle pazienti ultraottantenni. Per queste ultime si prevede infatti un aumento del 7% circa rispetto ai tassi osservati nel periodo 2015-2019.
Questi risultati provengono da uno studio in cui si sono stimati i tassi di mortalità per tumore nell’UE [1] e nel Regno Unito per il 2025. I risultati dello studio, condotto da ricercatori dell’Università degli Studi di Milano in collaborazione con l’Università di Bologna, sono stati pubblicati oggi sulla rivista Annals of Oncology [2].
Gli epidemiologi coordinati da Carlo La Vecchia, professore di statistica medica ed epidemiologia all’Università Statale di Milano, ritengono che un motivo per l’aumento dei tassi di mortalità per tumore della mammella tra le pazienti più anziane nell’UE possa essere dovuto alla mancanza di screening regolari e di diagnosi tempestive per le donne ultraottantenni, che hanno anche minore probabilità di ricevere i trattamenti più innovativi.
“Le donne anziane non sono incluse nei programmi di screening e probabilmente, rispetto alle donne più giovani, hanno minore giovamento dagli importanti progressi nella diagnosi e nella gestione del tumore della mammella, compresi i miglioramenti nella chemioterapia, nella terapia ormonale e nell’immunoterapia che include il trastuzumab e i farmaci similari, ma anche nella radioterapia e nella chirurgia” ha dichiarato La Vecchia.
L’aumento della prevalenza di sovrappeso e obesità osservato negli ultimi decenni nella maggior parte dell’Europa settentrionale e centrale ha portato a un aumento del rischio di tumore della mammella. Questo fenomeno, però, non è stato controbilanciato da un miglioramento della diagnosi e della gestione della malattia nelle donne anziane e, di conseguenza, potrebbe spiegare l’aumento della mortalità stimato.
Il gruppo di ricercatori prevede una diminuzione dei tassi di mortalità per tumore della mammella a tutte le età pari al 3,6% nell’UE e allo 0,8% in Italia nel 2025 rispetto al 2020. Il tasso di mortalità standardizzato per età è 13,3 per 100.000 donne nell’UE (per un totale di 90.100 decessi) e di 14,0 per 100.000 donne in Italia (per un totale di 13.660 decessi).
“Stimiamo che tra il 1989 e il 2025 siano stati evitati 373.000 decessi per tumore della mammella nell’UE. La maggior parte di questi decessi evitati è dovuta al miglioramento della gestione della malattia e all’introduzione di innovazioni terapeutiche, ma il 25-30% è probabilmente attribuibile auna maggiore diffusione della diagnosi precoce e del programma di screening. Poiché oggi il tumore della mammella può essere curato efficacemente grazie ad approcci innovativi, è essenziale che tutte le pazienti alle quali viene diagnosticato vengano indirizzate a centri oncologici in grado di offrire tutte le terapie necessarie. Inoltre, come indicato dagli andamenti sfavorevoli per le donne ultraottantenni, il controllo del sovrappeso e dell’obesità rimane una priorità, non solo per le malattie cardiovascolari, ma anche per i tumori, compreso il quello della mammella” ha aggiunto il professor La Vecchia.
I ricercatori hanno analizzato, per il quindicesimo anno consecutivo, i tassi di mortalità per tumore nell’UE [3] e nel Regno Unito, esaminando separatamente i tassi di mortalità per tumore dello stomaco, colon-retto, pancreas, polmone, mammella, utero (compresa la cervice), ovaio, prostata e vescica, nonché i tassi di mortalità per leucemie, per entrambi i sessi [4]. Sono stati raccolti i dati di mortalità dai database dell’Organizzazione Mondiale della Sanità e delle Nazioni Unite, relativi al periodo 1970-2020. Tali stime si sono dimostrate affidabili nel corso degli anni.
Tutti i tumori:
Nei Paesi dell’UE si prevede un calo del 3,5% circa dei tassi di mortalità per tutti i tumori: si passerà da 125/100.000 nel 2020 a 121/100.000 nel 2025 per gli uomini, e da 80/100.000 a 79/100.000 per le donne. In totale si stima che nel 2025 circa 1.280.000 persone moriranno di tumore nell’UE e circa 176.000 in Italia. In Italia il tasso di mortalità per tutti i tumori diminuirà per gli uomini, passando da 112 nel 2020 a 96/100.000 nel 2025, e per le donne, passando da 75 a 71/100.000.
Secondo le stime dei ricercatori, dal 1988 al 2025 nell’UE si sono evitati 6,8 milioni di decessi per tutti i tipi di tumore (4,7 milioni negli uomini e 2,1 milioni nelle donne), ipotizzando che i tassi di mortalità rimanessero costanti rispetto a quelli del 1988.
Tuttavia, a causa del crescente numero di anziani nella popolazione, il numero di decessi per tumore aumenterà da 671.963 nel 2020 a 709.400 nel 2025 tra gli uomini nell’UE e da 537.866 a 570.500 tra le donne. In Italia, invece, il numero di decessi passerà da 97.866 a 94.740 per gli uomini e da 79.991 a 81.740 per le donne.
Si prevede che i tassi di mortalità per la maggior parte dei tumori diminuiranno quest’anno nell’UE, a eccezione del tumore del pancreas, che mostrerà un aumento del 2% negli uomini e del 3% nelle donne. Per le donne si prevede un aumento del 4% del tumore del polmone e del 2% del tumore della vescica.
In Italia gli unici tassi di mortalità previsti in lieve aumento sono quelli per il tumore del pancreas e della vescica nelle donne. I tassi di mortalità per tutti gli altri tipi di tumore sono in calo per entrambi i sessi.
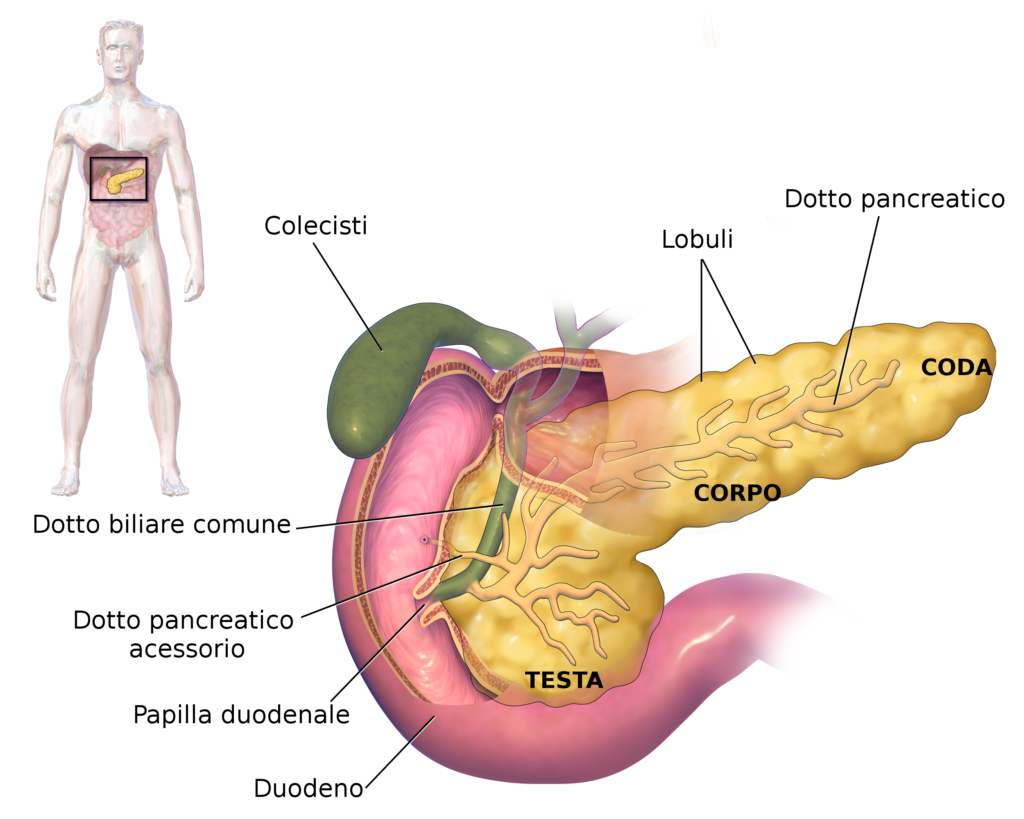
“Il fumo rimane di gran lunga la principale causa nota di tumore del pancreas, causando dal 20 al 35% dei casi in varie fasce di età, a seconda delle diverse abitudini di fumo. Il diabete, il sovrappeso che portano allo sviluppo della sindrome metabolica sono responsabili di circa il 5% dei tumori al pancreas in Europa. Questo aspetto sta diventando sempre più importante a causa della crescente prevalenza dell’obesità, ma il controllo e la prevenzione del fumo rimangono la priorità per il controllo anche del tumore del pancreas” ha spiegato la professoressa Eva Negri, docente di epidemiologia ambientale e medicina del lavoro dell’Università di Bologna e co-leader della ricerca.
Il tumore del polmone rappresenta la principale causa di morte per tumore tra gli uomini nell’UE (151.000 casi) e in Italia (19.600 casi). Nel nostro Paese il tumore della mammella è la prima causa di morte per cancro fra le donne italiane (13.660 casi). Anche nell’UE, il tumore della mammella rappresenta la principale causa di morte per tumore tra le donne; tuttavia, si stima che il tasso di mortalità per il tumore del polmone supererà quello della mammella nel 2025. Infatti, l’andamento della mortalità per tumore del polmone è ancora in aumento tra le donne (+3,8% rispetto al 2020).
Conclude Carlo La Vecchia: “Gli andamenti di mortalità per tumore continuano a essere favorevoli in tutta Europa. Tuttavia vi sono anche aspetti negativi: uno di questi sono i decessi per tumore del colon-retto nelle persone di età inferiore ai 50 anni, che hanno iniziato ad aumentare nel Regno Unito e in diversi Paesi dell’Europa centrale e settentrionale, a causa dell’aumento della prevalenza del sovrappeso e dell’obesità nei giovani che, per età, non sono coperti dallo screening del tumore colorettale. Inoltre i tassi di mortalità per il tumore del pancreas non sono in diminuzione nell’UE ed è ora la quarta causa di morte per tumore dopo il cancro del polmone, del colon-retto e della mammella. I tassi di mortalità per tumore del polmone stanno iniziando a stabilizzarsi, ma non ancora a diminuire nelle donne dell’UE. Le tendenze del tumore del pancreas e del polmone nelle donne sottolineano l’urgenza di attuare un controllo ancora più rigoroso del tabacco in tutta Europa”.
Il progetto è stato sostenuto dalla Fondazione AIRC; Claudia Santucci e Carlo La Vecchia hanno ricevuto sostegno dall’iniziativa Next Generation EU-MUR PNRR Extended Partnership Inf-Act.
NOTE
[1] Al momento di questa analisi, l’UE contava 27 Stati membri, con l’uscita del Regno Unito nel 2020. Cipro è stato escluso dall’analisi perché non erano disponibili sufficienti dati a lungo termine, necessari per prevedere le tendenze, soprattutto nei piccoli Paesi. Tutti gli altri Paesi avevano dati che risalivano almeno al 1970.
[2] “European cancer mortality predictions for the year 2025 with focus on breast cancer”, by C. Santucci et al. Annals of Oncology, doi: 10.1016/j.annonc.2025.01.014.
[3] I tassi standardizzati per età per 100.000 abitanti riflettono la probabilità annuale di morire aggiustata per riflettere la distribuzione per età di una popolazione.
[4] Il documento contiene tabelle individuali dei tassi di mortalità per tumore per ciascuno dei sei massimi Paesi Europei.

Testo dall’Ufficio Stampa Direzione Comunicazione ed Eventi istituzionali Università Statale di Milano e dall’Ufficio Stampa dell’Università degli Studi di Bologna.