I RICERCATORI DI UNITO SCOPRONO UNA PROTEINA FONDAMENTALE PER LO SVILUPPO DEL TUMORE DEL PANCREAS
Lo studio, pubblicato dalla prestigiosa rivista Gastroenterology, è importante per comprendere a fondo la patologia e per identificare possibili marker molecolari utili sia nella diagnostica sia nella terapia
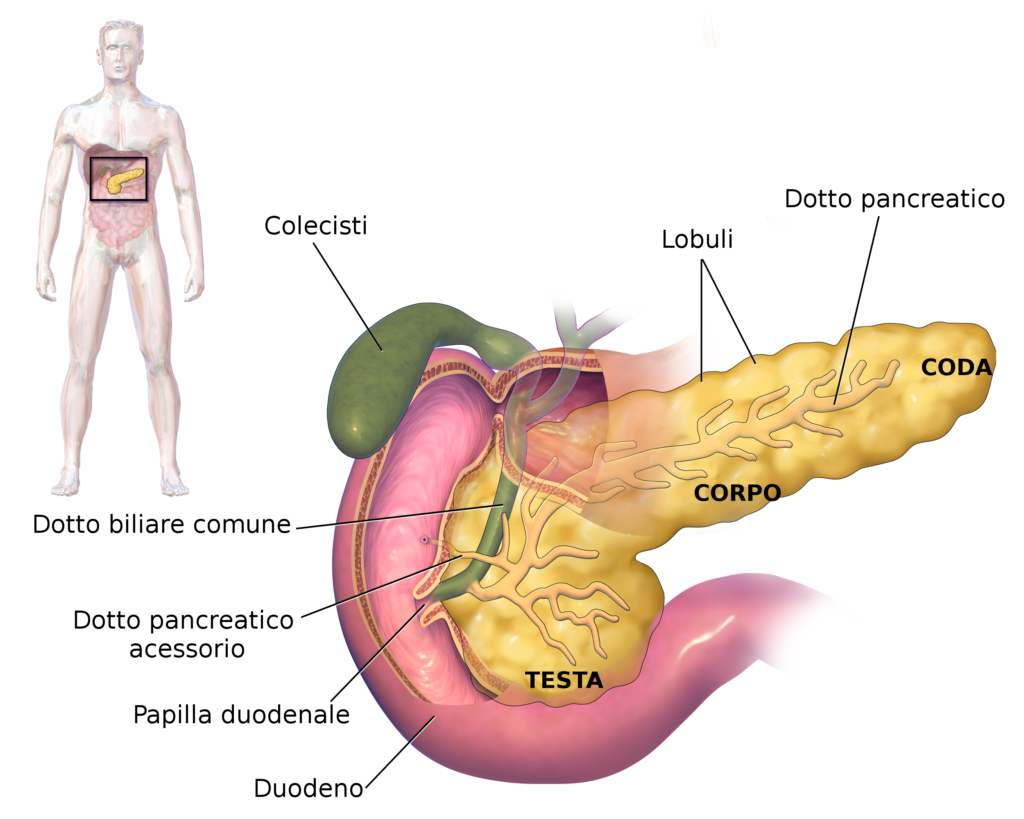
Gli scienziati del Centro di Biotecnologie Molecolari dell’Università di Torino hanno scoperto un fattore indispensabile per l’insorgenza del tumore al pancreas, identificato nel ruolo della proteina chiave p130Cas. Il loro studio è stato pubblicato dalla prestigiosa rivista Gastroenterology.
Il tumore al pancreas rimane a oggi uno dei tumori più letali e complessi da individuare: la scarsa percentuale di sopravvivenza è principalmente dovuta al fatto che la malattia, nelle sue fasi iniziali, non si manifesta con sintomi eclatanti. Inoltre, la comprensione di tali fasi è ancora limitata, così come la conoscenza di marcatori molecolari per la diagnosi precoce. I tumori pancreatici hanno origine a partire dalle cellule esocrine, responsabili della produzione degli enzimi pancreatici, che permettono la digestione: tali cellule possono andare incontro a una metaplasia acino-duttale (termine che indica la trasformazione di una tipologia cellulare in un’altra differente), che rappresenta il primo step nella progressione tumorale sostenuta dall’oncogene Kras. Gli oncogeni sono geni che, se subiscono delle mutazioni, causano lo sviluppo del tumore; in più del 90% dei tumori pancreatici sono state infatti individuate mutazioni di Kras. Tramite screening genetici ad ampio spettro, la proteina adattatrice p130Cas è emersa come un potenziale interattore di Kras e possibile candidato per predire la suscettibilità allo sviluppo del tumore pancreatico.
Coordinati dalle Prof.sse Miriam Martini e Sara Cabodi, i ricercatori di UniTo hanno analizzato campioni umani di tumore pancreatico e generato modelli murini di cancro del pancreas di crescente aggressività per studiare la relazione fra p130Cas e la tumorigenesi nel pancreas.
Il Dott. Andrea Costamagna, primo autore dello studio, utilizzando topi suscettibili al tumore al pancreas e privi della proteina p130Cas ha osservato che un’elevata espressione di p130Cas è frequente nel tumore pancreatico e ha quindi una stretta correlazione con un maggiore sviluppo del tumore e una peggior prognosi. Al contrario, i topi in cui p130Cas è stata rimossa non sviluppano il tumore nonostante l’attivazione dell’oncogene Kras. Nello studio si è dimostrato che la delezione di p130Cas sopprime la tumorigenesi, poiché blocca la metaplasia acino-duttale tramite l’inibizione della via di segnalazione PI3K-AKT, coinvolta nei meccanismi di crescita e sopravvivenza e fondamentale per la progressione tumorale.
Grazie a una stretta collaborazione con la Prof.ssa Elisa Giovannetti del VU University Medical Center di Amsterdam, è stato inoltre possibile dimostrare che l’elevata espressione di p130Cas si correla a una peggior prognosi e a una minore aspettativa di vita dei pazienti. Queste scoperte hanno dimostrato come p130Cas agisca a valle di Kras per aumentare la segnalazione di PI3K-AKT richiesta per la metaplasia acino-duttale e il successivo sviluppo del tumore, facendo inoltre luce su aspetti ancora poco chiari dello sviluppo del tumore al pancreas oltre ad aprire la strada per futuri studi volti a comprendere se la proteina p130Cas potrà essere utilizzata come marcatore molecolare per l’individuazione di questo tumore tristemente ancora troppo letale.
La scoperta di proteine chiave che regolano le fasi iniziali della tumorigenesi è fondamentale per comprendere a fondo questa patologia e identificare possibili marker molecolari utili nella diagnostica e nella terapia.
Testo dall’Ufficio Stampa dell’Università degli Studi di Torino






